细胞实验(一)基本操作
以下是悬浮细胞(如淋巴细胞、某些肿瘤细胞系)的 复苏、传代、换液、冻存 基本操作步骤及注意事项:
一、细胞复苏
目的
快速恢复冻存细胞的活性。
步骤
准备
- 预热完全培养基至37℃,离心机预冷至4℃。
- 水浴锅预热至37℃。
解冻
- 从液氮中取出冻存管,迅速放入37℃水浴,轻轻摇晃至完全解冻(约1-2分钟)。
清洗
- 将细胞悬液转移至15ml离心管,加入5ml预冷的完全培养基(中和DMSO毒性)。
- 4℃、200×g离心5分钟(即低速离心机1000rpm),弃上清。
重悬与接种
- 用适量完全培养基轻柔重悬细胞,计数后接种至培养瓶/皿。
- 放入37℃、5% CO₂培养箱,24小时后观察细胞状态。
注意事项
- 操作迅速,避免反复冻融。
- 初次复苏建议培养基中加1-2倍双抗(防止污染)。
二、细胞传代
目的
维持细胞生长密度,防止过度堆积。
步骤
收集细胞
- 轻摇培养瓶使细胞均匀悬浮,将细胞悬液转移至离心管。
- 室温、200×g离心5分钟,弃上清。
计数与稀释
- 用完全培养基重悬细胞,按比例稀释(如1:3或1:4)。
- 接种至新培养瓶,补足培养基(根据细胞类型调整密度)。
培养
- 放回培养箱,定期观察细胞增殖状态(通常2-3天传代一次)。
注意事项
- 离心速度不宜过高(避免机械损伤)。
- 传代密度需优化(过高易聚集,过低生长缓慢)。
三、细胞换液
目的
清除代谢废物,补充营养。
步骤
离心
- 将细胞悬液转移至离心管,室温、200×g离心5分钟,弃上清。
换液
- 用预热的完全培养基重悬细胞,接种回原培养瓶或新瓶。
注意事项
- 若细胞状态良好,可直接补充新鲜培养基(无需离心)。
- 换液频率根据细胞代谢速度调整(通常2-3天一次)。
四、细胞冻存
目的
长期保存细胞活性。
步骤
准备冻存液
- 配方:完全培养基 + 10% DMSO + 20% FBS(或商品化冻存液,可以直接冻存在-80℃,不用梯度降温)。
- 预冷至4℃。
收集细胞
- 取对数生长期细胞,离心后弃上清,用冻存液重悬至1-5×10⁶ cells/ml。
分装
- 将细胞悬液分装至冻存管(每管1-1.5ml),标记名称、日期、代数。
程序降温
- 冻存盒法:4℃ 30分钟 → -20℃ 2小时 → -80℃过夜 → 转移至液氮。
- 或使用程序降温仪(每分钟降1℃至-80℃)。
注意事项
- DMSO对细胞有毒,操作需快速。
- 冻存前检测细胞活力(>90%为宜)。
关键通用原则
- 无菌操作:全程超净台内完成,避免污染。
- 轻柔操作:吹打、离心时避免机械损伤。
- 记录信息:冻存/复苏时记录细胞代数、日期、培养基批次。
- 质量控制:定期检测支原体污染及细胞活性。
常见问题处理
| 问题 | 可能原因 | 解决方案 |
|---|---|---|
| 复苏后细胞死亡率高 | 解冻速度慢/DMSO残留 | 快速解冻,彻底清洗冻存液 |
| 传代后细胞不增殖 | 密度过低/培养基失效 | 调整接种密度,更换新鲜培养基 |
| 冻存后无法复苏 | 降温速率不当/液氮泄漏 | 检查冻存程序,确保液氮储存 |
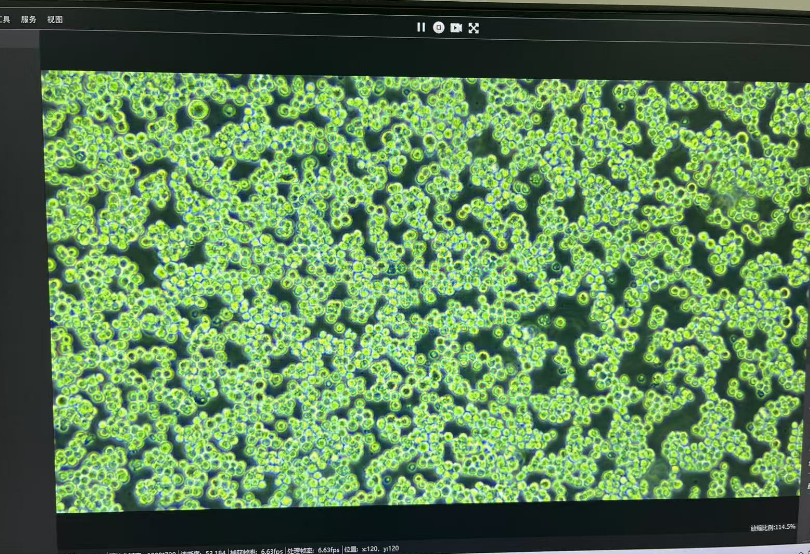
【细胞状态佳,密度均匀,边界清晰、透亮、光滑】
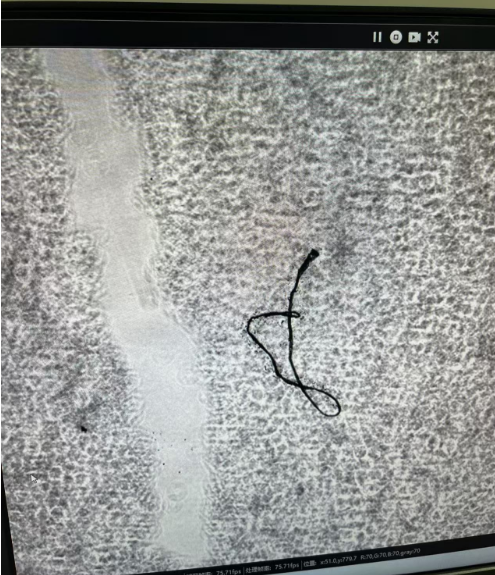
【细胞污染】
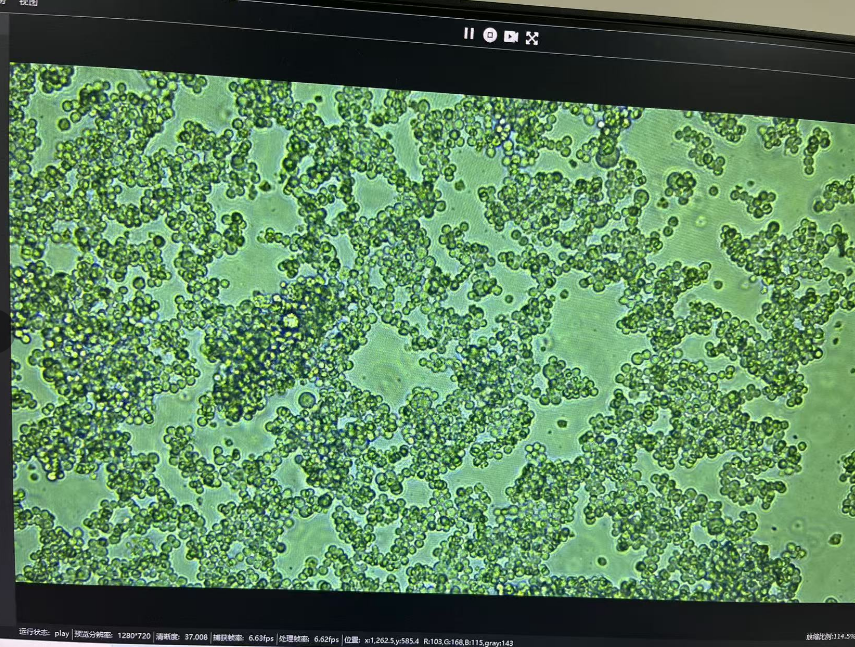
【细胞结成团块】
本博客所有文章除特别声明外,均采用 CC BY-NC-SA 4.0 许可协议。转载请注明来源 Rio!
